中国女孩,终于不用去国外打疫苗了。7月17日,葛兰素史克(GSK)宣布其产品Cervarix(希瑞适)(人乳头状瘤病毒疫苗HPV [16 型和 18 型])获得中国食品药品监督管理总局的上市许可,成为国内首个获批的预防宫颈癌的 HPV 疫苗。
但是在欢呼雀跃之余,我们不禁感叹,为什么这种可以挽救数百万妇女生命的疫苗,在中国的上市却要晚10年。在全球160多个国家都已经将这种药物纳入公共卫生防控体系的时候,它在新加坡、日本等亚洲国家都已经被证明安全有效的时候,中国却还纠结在这种药物是不是适合中国人而担忧。
或许这种担忧本身也只是一种说辞,更多的是对监管权力的迷恋和蛮横,而这带来的结果,并不是更安全高效的药物体系,付出的却是众多患者的健康乃至生命的代价。
作为一种人类第一能够用来消灭癌症的疫苗,宫颈癌疫苗已经问世了十年。
2006年,默沙东公司研发出全球第一个HPV疫苗“佳达修”(gardasil),这款四价疫苗防治HPV16、18、6、11型病毒。随后,葛兰素史克也生产了二价疫苗“希瑞适”(cervarix),针对HPV16和18,随即也开始上市。
后来默沙东又推出了GARDASIL9(佳达修9,九价重组人乳头状瘤病毒疫苗)也得到了FDA的批准。
截至目前,该疫苗已在全球160多个国家和地区获批上市,包括中国的台湾、香港和澳门地区。
为什么这种药物可以在其他国家上市比较快,这是因为作为药物评审的黄金标准,一种药物只要通过了FDA的审批,在全球大多数国家可以直接进入临床应用,但依据中国内地的规定,药物进入中国内地必须要有中国人的临床研究。
根据《药品进口管理办法》,进口疫苗必须在国内重新开展临床试验,获得中国药监局下发的《进口药品注册证》后才可以上市。也就是说,要再做一次专属于中国人的三期临床试验。
而且疫苗的临床试验还跟一般药物的临床试验不同,要看出其保护效果不是那么容易,即便实验顺利,也需要3到6年才能看出效果。
按照流程来说,一种进口新药仅从申请到获批进行临床试验,到最终被中国内地患者使用平均需要5年,如果再算上纳入医保目录所需的时间,平均则需要等6~8年。而HPV疫苗,则用了整整10年。
有人做过一个简单的计算。根据2011年卫生部数据,中国每年有约3万名妇女死于宫颈癌,新发病例13.2万。那么宫颈癌疫苗晚上市10年,造成13.2X10=132万花季少女和年轻妈妈罹患宫颈癌而遭受病痛折磨!宫颈癌疫苗晚上市10年,更造成30万花季少女和年轻妈妈命丧黄泉!
虽然这个计算肯定不准确,即便是HPV疫苗上市了,也不能说完全消灭宫颈癌,但是每年发病和死亡的数字,肯定会大大降低。
国际上普遍认定,HPV疫苗对9-45岁的女性都有预防效果,如果女性能在首次性行为之前注射HPV疫苗,会降低90%的宫颈癌及癌前病变发生率。
中国医学科学院、北京协和医学院肿瘤研究所的王少明博士在《vaccine》发表的论文曾经估算,若我国HPV疫苗项目的接种对象为9~15岁女孩,2006年至2012年7年HPV疫苗的免疫接种延迟,可能造成我国5900万女孩错失接种良机。若这部分女孩未来不接受筛查等其他干预措施,她们中将出现38万的宫颈癌新发病例和21万宫颈癌死亡病例。
但是在监管部门眼中,这或许就只是一组数字而已。他们要履行的是自己的责任,行使的是自己的权力,他们所关心的,是在自己的位置上不要出事。
尤其在原国家药监局局长郑筱萸被判死刑,近年来外资药企的贿赂风波之后,官员们对新药的审批变得更为小心翼翼,对一些新药宁可不批,也绝不能犯错误,这自然让新药的审批更为艰难。
任何药物都要针对中国人重做临床试验,当然可以说是出于安全性和有效性的考虑,但是中国人的体质到底有多么特殊,即便是在全球已经证明安全有效,在亚洲地区也证明安全有效都不行?
在上世纪八、九十年代,日本也曾对欧美研发的新药较为担心,因为这些新药的临床实验对象主要是白种人,但后来的研究数据证明不同人种之间确实可能存在某些方面的差异,但只有极少数药物需要考虑到种族之间的差异,绝大部分药物都可以忽略不计。
在进入本世纪之后,日本曾经对欧美新药设置的一些门槛逐渐消除了。
实际上,早在2002年至2005年期间,默沙东和葛兰素史克就在中国台湾等亚洲地区进行过大规模临床试验,在美国宫颈癌疫苗的实验也相当全面,美国人中华裔和亚洲人群也占有一定比例。这也是FDA给予疫苗批准所考虑的一个重要方面。
大多数国家均采纳了FDA的结论,在中国香港,医药公司只需给卫生局提供已上市国开具的证明,最多一年即可通过审批。但中国内地就是不承认。
有人评论说,现在,HPV疫苗已在160多个国家和地区上市,我们国家竟然落后于160个国家和地区!清朝建设第一条铁路也没有落后世界160多个国家和地区!我们不得不承认残酷的现实:我们的疾病预防比清朝还落后!
今天科学网上有一篇文章,似乎可以帮着中国药监部门撑一下腰。这篇文章中说,在媒体的宣传报道中,有一个真相从未被提及,获批的HPV疫苗希瑞适在中国达不到其在欧美的同等效果!
这篇文章提出的理由是,高危型HPV病毒主要有HPV16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59和68型。根据欧美流行病学数据,70%的宫颈癌与HPV16和HPV18相关。
而这次上市的希瑞适,就是针对HPV16和HPV18的二价疫苗,而覆盖HPV16、18、6、11的来自默沙东的佳达修及佳达修9,尚未被批准上市。
根据作者的分析,在中国人群中,感染率最高的高危型HPV病毒是HPV16、HPV52和HPV58。也就是说,现在上市的疫苗,管得了HPV16,管不了HPV52和HPV58。针对中国人群的宫颈癌预防,还是得来9价疫苗!
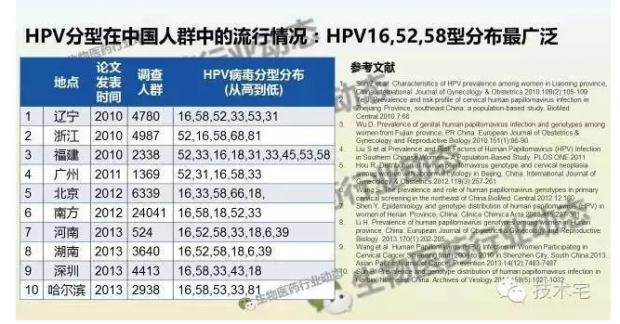
实际上,作者只是根据文献做了一个简单的排序,发现排在前三位的是16,52,和58,而18确实是不多见。但是从这个排序上,也可以看出,HPV16的占比是最高的。
作者并未指出HPV16的占比由多高,因为说出来如果HPV占比很高,52和58的占比很低的话,也就没法支持他的结论了。
实际上,根据中国医学科学院/北京协和医学院肿瘤研究所流行病学研究室主任乔友林的研究,国内84%的宫颈癌患者病因是感染HPV16或18,这甚至超过国际平均水平。
如果按照乔友林教授的统计,二价疫苗在中国上市,其实比在欧美国家更有用。
当然任何一种疫苗的作用,也不能被夸大成100%有效,这是不可能的,二价疫苗已经能够用于预防第一多的HPV16型病毒,比根本没有要好得多。70%有效就够好了,和80%有效也没有本质的区别。
实际上,在我看来,这种差异更多是来自生活习惯和生活环境的差异,也跟人种无关。
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 